Boletín
Nº 202 - octubre 2019
Un nuevo editor CRISPR podría
corregir casi todas las enfermedades genéticas
Un equipo científico del Broad Institute en EE UU ha presentado una nueva herramienta de edición
de ADN de alta precisión que, según los autores, podría corregir el 89 % de las
variantes genéticas humanas conocidas asociadas a enfermedades. Todo ello, sin
los efectos secundarios de
Ana Hernando
| | 22 octubre 2019 12:47
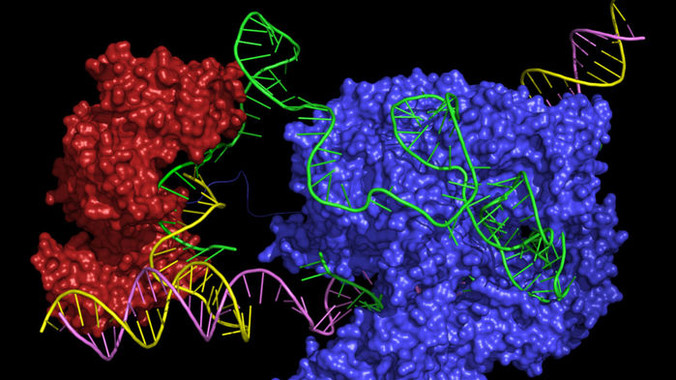
El prime editor une dos enzimas, Cas9
(azul) y transcriptasa inversa (roja), a un ARN guía (verde) que lleva el
complejo a un lugar específico en la doble hélice del ADN (amarillo y púrpura)
y también contiene el código para la inserción de ADN nuevo en ese punto / Peyton Randolph
La revista Nature presenta esta semana un estudio liderado por David Liu en Broad
Institute, un centro mixto de la Universidad de Havard y del MIT, que asegura haber desarrollado una
potente herramienta de edición molecular capaz de modificar con una precisión
sin precedentes el ADN de las
células humanas, con menos efectos secundarios y errores que otras técnicas
actuales.
|
Según los autores, las
limitaciones del famoso sistema CRISPR
Cas9 incluyen la ruptura de doble cadena en el ADN, lo que conduce a
mezclas incontroladas de inserciones y deleciones y
la baja eficiencia de la corrección de la edición genética. En la actualidad,
se conocen unas 75.000 variantes genéticas humanas asociadas a enfermedades
que no pueden ser corregidas eficientemente con las técnicas disponibles.
La herramienta desarrollada por el
equipo de Liu, llamada prime editing o edición de calidad,
evita las rupturas de ADN de doble cadena y, en principio, "podría corregir alrededor
del 89 % de las variantes genéticas humanas conocidas asociadas a
enfermedades", indican los científicos.
|
|
Cuadro de datos
|
|
Los investigadores realizaron más de 175 ediciones en células La
herramienta evita las rupturas de ADN de doble cadena y permite realizar
la edición genética con menos errores y efectos secundarios que Cas9
|
|
|
|
|
|
|
|
|
|
Para
lograrlo, el equipo combinó la enzima Cas9 con una segunda enzima llamada transcriptasa inversa. La máquina molecular
resultante -cuando se combina con un ARN guía- puede buscar un sitio en el ADN
específico y, al mismo tiempo, hacer que la nueva información genética editada
reemplace la secuencia de ADN concreta, pero corta una sola hebra de ADN
modificada para evitar mutaciones.

David Liu / Casey Atkins Photography
(Broad Institute)
Resultados espectaculares
"De esta
forma, el grupo de Liu ha conseguido, con resultados
espectaculares, editar secuencias sin necesidad de un corte de doble cadena de
ADN, uno de los riesgos de la edición genética con las distintas herramientas
disponibles", comenta a Sinc Guillermo Montoya, investigador experto en CRISPR en la Novo Nordisk Foundation Center for Protein Research,
en la Universidad de Copenhague, que no ha participado en este estudio.
|
Los investigadores realizaron más de 175 ediciones en
células humanas, incluida la corrección de las causas genéticas de la anemia de células falciformes y de la
enfermedad de Tay-Sachs.
Los resultados apuntan a que "la técnica es más eficaz, produce menos efectos
indeseados y tiene menos edición errónea que la llevada a cabo con Cas9".
"Se puede pensar en el prime editor como un procesador de
texto, capaz de buscar secuencias concretas de ADN y de forma muy precisa
reemplazarlas con secuencias de ADN editadas", explicó Liu
en rueda de prensa.
Los
autores también señalan que la nueva técnica aún necesita más investigación
para comprender sus efectos y mejorar sus capacidades.
|
|
Cuadro de datos
|
|
Los investigadores realizaron más de 175 ediciones en células
humanas, incluida la corrección de las causas genéticas de la anemia de
células falciformes
|
|
|
|
|
|
|
|
|
|
En opinión de Montoya, la propuesta de Liu
y su equipo "es novedosa, prometedora y aporta una nueva herramienta para
edición genética. Sin embargo, "desde el punto de vista estructural resulta
bastante compleja y habrá que ver si puede ser empleada de forma general. Creo
que en el futuro no habrá una única tijera molecular y que se desarrollarán
distintas herramientas que se emplearán dependiendo del tipo de edición que se
quiera realizar", resalta.
|
Cuadro
de datos
|
Referencia bibliográfica:
Andrew V. Anzalone,
Peyton B. Randolph, Jessie R. Davis, Alexander A. Sousa, Luke W. Koblan, Jonathan M. Levy, Peter J. Chen, Christopher
Wilson, Gregory A. Newby, Aditya Raguram, David
R. Liu. "Search-and-replace genome editing without
double-strand breaks or donor DNA". Nature (21 de noviembre, 2019)
|
|
|
Zona geográfica:
Norteamérica
Fuente:SINC
|

|